
【编者按】现如今,随着人们生活质量的提高,亦愈重视其身体的康健,防患于未然,就显得尤为重要。《黄帝内经》有言:“上工治未病,不治已病,此之谓也。”“治未病”即采取相应的措施,防止疾病的发生发展。疫苗的发现便很好的印证了这一观点。宫颈癌作为妇科最常见的恶性肿瘤,在我国的发病率亦呈现上升趋势。HPV疫苗的接种则有效的预防了宫颈癌的发生。接下来,让我们跟随天津医科大学总医院薛凤霞教授一起走进后疫苗时代。
一、背景
1.宫颈癌是由高危型人乳头瘤病毒(HR-HPV)在女性生殖道持续性感染引起的疾病。近年,我国宫颈癌发病呈上升趋势,平均每年上升11.3%。2015年,我国肿瘤登记年报显示:宫颈癌新发病例数达9.89万,死亡病例数达3.05万。中国的宫颈癌筛查面临的形势非常严峻。
2. 宫颈癌筛查可以早期发现宫颈CIN病变,降低疾病负担,属于二级预防;HPV疫苗的接种主要作用是降低HPV感染,从一级预防角度预防宫颈癌的发生。
二、宫颈癌现行筛查方法与策略
现在宫颈癌筛查推荐比较多的是:细胞学筛查、HR-HPV初筛、细胞学联合HR-HPV筛查。
1. 单一细胞学筛查:起始年龄21岁。
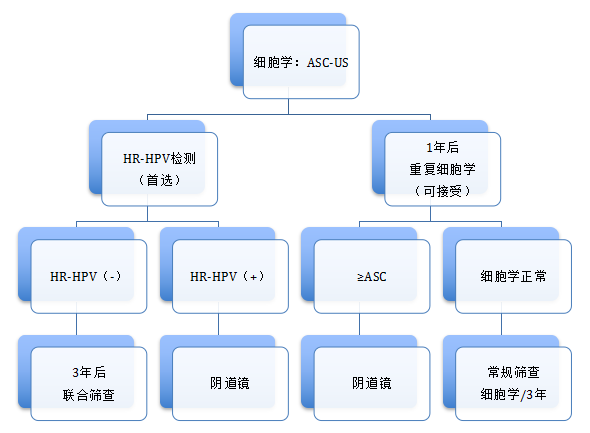
细胞学筛查的特点是:敏感度不高,但是特异性比较高。细胞学筛查处理的难点在于对于细胞学筛查结果ASC-US的处理。如果是ASC-US以上级别的病变,建议阴道镜检查。
对于普通人群ASC-US的管理:首选进行HR-HPV检测来做分流,如果是依从性非常好,也可以1年以后重复细胞学检查。对于围绝经期和绝经后年龄的女性,首选HPV检测做分流。
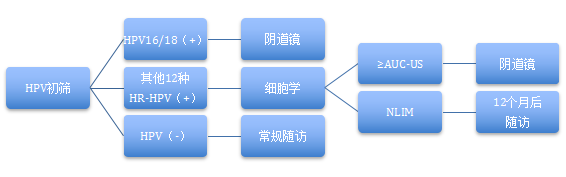
2. HR-HPV初筛处理流程
HPV16/18阳性,直接进行阴道镜检查。如果是其他HR-HPV阳性,可以用细胞学筛查做分流,出现ASC-US以上级别的病变,建议阴道镜检查,如果未见上皮内病变/恶性细胞(NLIM),12个月后随访;如果初筛HR-HPV阴性,常规随访即可。
HPV作为初筛检查,敏感性高,但是特异性低,所以确定初筛年龄很重要。
· 2015年,美国ASCCP过渡期指南指出:高危型HPV检测用于宫颈癌初筛查可用于25岁以上女性。
· 2016年EUROGIN Roadmap提出:基于HPV检测的宫颈癌筛查起始年龄为30-35岁。
· 中国单独HPV筛查年龄定为30岁。
3. 细胞学联合HR-HPV筛查:起始年龄30岁。
筛查4种结果的处理:
(1)HPV和细胞学均阴性,每5年联合筛查一次。
(2)HPV阳性且细胞学ASC-US及以上,直接阴道镜检查。
(3)HPV阳性但细胞学阴性,建议12个月后重新联合筛查或HPV16/18阳性需转诊阴道镜。
(4)HPV阴性但细胞学ASC-US及以上:ASC-US,每三年一次联合筛查(国内实际操作,受限于病理医生水平,一般定为6-12个月后复查);LSIL、HSIL以及SCC女性,必须行阴道镜检查。
4. 有一些问题值得我们讨论:
目前宫颈癌3种筛查方案中,出现HPV16/18阳性者,均直接转诊阴道镜,但是转诊阴道镜的HR-HPV型别仅仅定为16/18是否适合我国?
有争议的部分在于18型别要做阴道镜检查,但是对于HSIL、LSIL中发病率在18型别之前的型别,如果不做阴道镜检查,是否存在漏诊可能呢?
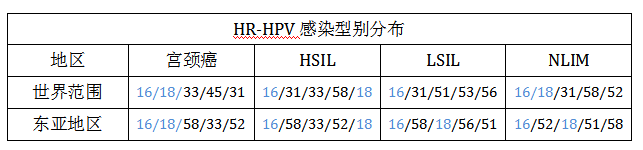
HR-HPV感染型别分布
HR-HPV在国外和国内一些地区的感染型别分布如下:
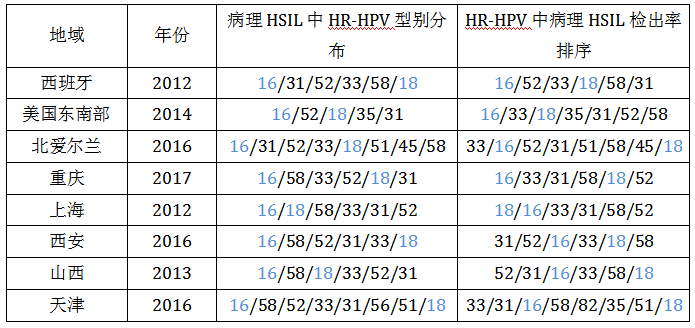
在我国,宫颈活检病理为HSIL患者中HR-HPV感染型别排序与国外并不完全一致:
-国内HPV16在HSIL中检出率最高,与国外一致;
-国内HPV18在HSIL中检出率不定;
-国内HPV58/52/33/31在HSIL中检出率较高。
我们目前需要提出的问题是:
除HPV16/18阳性外,HPV58/52/33/31阳性者转诊阴道镜能否减少漏诊?
三、HPV疫苗的前世今生
1. HPV疫苗目前有三种:
Cervarix希瑞适、Gardasil 4佳达修4、Gardasil 9佳达修9。
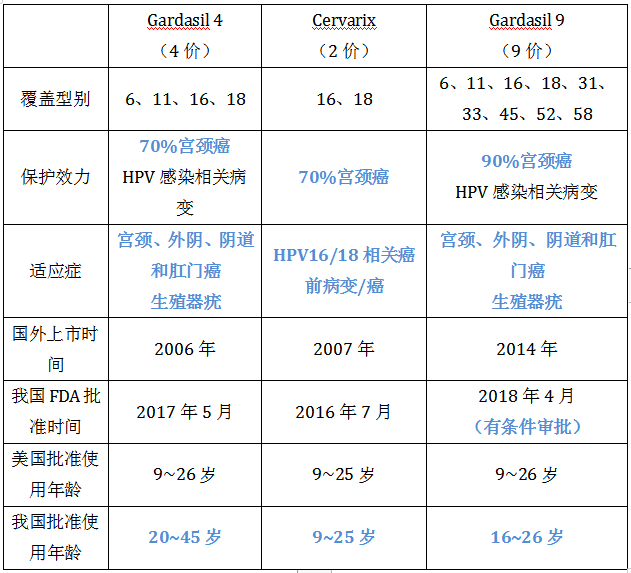
2. HPV疫苗接种现状
据WHO统计,截至2018年5月15日,全球有80个国家(41%)将HPV疫苗接种纳入国家免疫计划。在我国,HPV疫苗接种仍然是自费项目。
3. WHO推荐接种HPV疫苗——2017年5月《HPV疫苗:WHO立场文件》
· HPV疫苗应用作预防宫颈癌和HPV其他疾病综合协调策略的一部分,建议将HPV疫苗接种纳入国家免疫计划。
· 已上市的三种HPV疫苗均具有良好的安全性和有效性。
· 已上市的三种疫苗均为预防性HPV疫苗,对HPV感染及相关疾病的治疗作用不确定。
· 对未发生性生活的女孩进行接种,将获得最佳预防效果。
· 疫苗接种后仍需要进行宫颈癌筛查。
这里需要注意一点,对于年龄较大的育龄期女性,建议先做宫颈癌筛查,是规避风险,也是明确接种前就已经存在的感染和病变。
四、疫苗接种后筛查存在的困惑与挑战
(一)整体形势
1. 很多发达国家正在或已进入后疫苗时代。
2. 我国HPV疫苗接种尚处于起步阶段。
3. 后疫苗时代宫颈癌筛查中存在的问题将逐渐凸显并长期存在。
4. 疫苗接种后筛查中存在的困惑与挑战需未雨绸缪。
(二)在疫苗接种后可能在以下几个方面产生影响:
1.宫颈HSIL发生率降低。
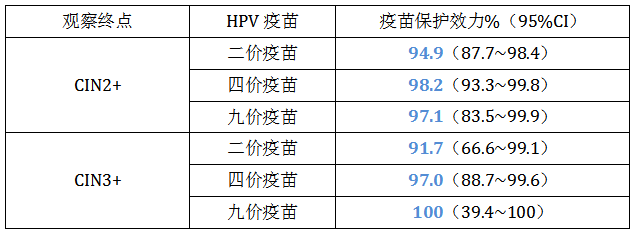
研究结果1
美国一项研究对HPV四价疫苗接种后HPV16/18相关宫颈高级别病变发生率进行分析显示:
2008~2012年期间,至少接种一剂疫苗的女性中,HPV16/18相关CIN2+病变发生率从53.6%显著下降至28.4%。
研究结果2
2000~2014年澳大利亚-维多利亚,HPV四价疫苗接种后,30岁之前的女性宫颈病变发生率大幅下降。
2.人群HPV感染型别流行趋势发生改变。
研究结果1
苏格兰于2008年将二价疫苗纳入国家免疫接种计划
该研究对2009~2013年苏格兰5765例20~21岁女性接种二价疫苗后HPV感染率进行统计,结果显示,HPV16、18、33、31、45感染率显著降低。虽然接种的只是二价疫苗,对于其他型别的感染率也有影响,考虑有交叉免疫保护的作用。
研究结果2
意大利巴西利卡塔地区自2007年起免费接种HPV四价疫苗
该研究比较接种疫苗组(1314例)接种5~7年后与未接种疫苗组(1479例)HPV感染率差异,结果显示:
未接种疫苗组,HPV感染率由高到低依次为16、42、52、31、51。
接种疫苗组,HPV感染率由高到低依次为42、51、39、52、31、58。
研究结果3
英国自2008年起将HPV疫苗纳入国家免疫计划
该研究比较HPV二价疫苗接种前与接种后2~3年、4~5年不同型别HPV感染率变化,结果显示:
对于免疫覆盖率较高的16~18年龄组,接种后2~5年HPV16/18感染率下降;免疫交叉保护作用使HPV31、33、45感染率下降。
各年龄组(16~18岁、19~21岁、22~24岁)其他型别HR-HPV感染率有所上升(24.9%升至33.7%、26.9%升至39.6%、26.4%升至32.9%)。
研究结果4
美国一项对全国健康与营养调查(NHANES)
2007~2012年20~26岁接种四价疫苗女性的数据分析显示:
接种疫苗者比未接种者HPV6、11、16、18感染率降低(7.4% vs 17.1%)
接种疫苗者比未接种者其他型别HR-HPV感染率高(52.1% vs 40.4%)
3.疫苗接种后对筛查策略的影响。
(1)随着HPV疫苗的推广,以单纯HPV16/18分型检测的初筛方法不再合适。
· 基于16/18阳性感染率下降,HPV16/18分型的效力可能会递减。
· HPV疫苗接种人群的筛查,细胞学和非分型的HPV检测效果较差。
· 后HPV疫苗时代,筛查方法的特异性要求更高。
(2)亟待结合我国自身特点,因地制宜,探索适用于我国的后疫苗时代筛查策略:
风险分层管理
同等风险同等管理——联合筛查5年CIN3+累积风险
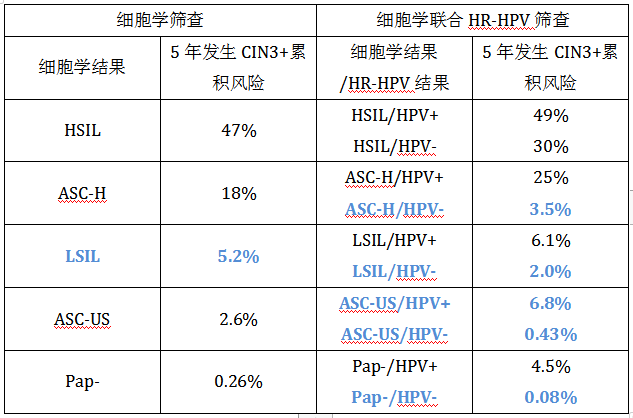
(3)HPV拓展分型检测
· 后疫苗时代,HPV16/18型外的其他高危型HPV分型正获得关注:
由于HPV疫苗接种使得未来HPV16/18感染率下降,因此其他非HPV16/18的高危亚型也应单独列出并单独报告,而非不分型集中一起报告。
· 尽管HPV16/18型是导致宫颈癌的最主要型别,但筛查目的是为了检出癌前高级别病变(CIN2和CIN3),HPV拓展分型具有更为重要的作用。
· 拓展分型可通过风险分层来提升HPV筛查的特异性,成为HPV初筛的应用趋势。
2018年,HPV拓展分型为:HPV16、18、31、52、45、51分型+另外三级高危型分级(33/58)、(39/68/35)、(59/56/66)。
(4)HPV分型检测对ASC-US的风险分层
· Schiffman等开展一项研究旨在通过HPV分型检测对细胞学ASC-US且HPV(+)的患者进一步风险分层:(研究人群为2007~2010年,KPNC注册的13890例HPV(+)细胞学ASC-US者,随访3年。HPV检测方法为BD Onclarity HPV分型检测)
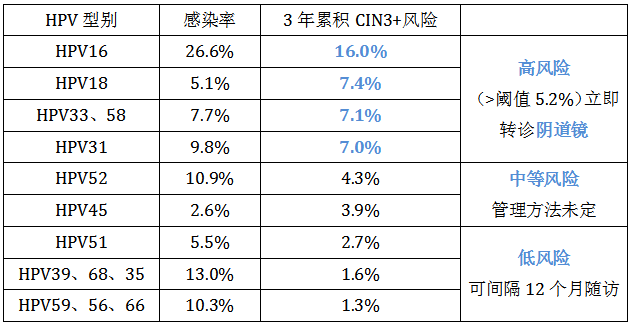
该研究认为,HPV分型检测对细胞学ASC-US者进一步分流管理,可减少约40%HPV阳性ASC-US者的立即阴道镜转诊。
· HPV分型检测可优化ASC-US的临床管理:
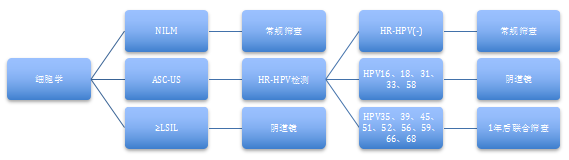
(5)精准筛查技术
·P16/Ki-67双染色法在ASC-US、LSIL分流的作用
Chen等对7项国外研究进行了荟萃分析,比较ASC-US、LSIL患者采用P16/Ki-67双染色法及HR-HPV检测进行分流的特异度、敏感度,结果显示,两种方法的敏感度相似(分别为91%、94%),而P16/Ki-67双染色法的特异度明显高于HR-HPV检测(分别为64%、35%),提示,P16/Ki-67双染色法可作为ASC-US、LSIL分流的策略之一。
· P16/Ki-67双染的应用
宫颈细胞共表达P16/Ki-67与存在CIN2+病变及HR-HPV持续感染显著相关。
通过P16/Ki-67免疫细胞化学染色的方法可对宫颈脱落细胞进行更为直观的检查和判断。
· 目前已陆续有研究提示对于HPV阳性,也可以对宫颈细胞涂片采用P16及Ki-67的双染进行分流,阳性者直接转诊阴道镜,阴性者1年后再次复查HPV。
· P16及Ki-67双染试剂盒在分流中具有较好的应用前景,目前需要考虑的是降低成本,开发国产相应的试剂,以便在国内推广中应用。
(三)疫苗接种后筛查存在的困惑与挑战
1. 目前,HR-HPV检测的敏感度高(88%左右),阴性预测值高(99%左右),并且客观性好,多应用于高收入国家。
2. 合格的病理医生培养周期长,培养成本高,从医疗经济/效益成本考虑,HR-HPV筛查可能更适合包括中国在内的细胞病理医生资源不足的国家。
3. 我国采用HR-HPV检测作为一线筛查存在的问题
· 国外应用于宫颈癌筛查的HR-HPV检测试剂有临床数据验证及严格质控。
· 我国目前HPV检测相关试剂多达100余种,但多数产品缺乏宫颈癌筛查的临床数据及随访数据的支持,且缺乏严格质控。
· 国家相关部门、企业以及医疗机构需共同进行多中心的临床验证,做好质控,在保证检测敏感度的同时,提高HPV筛查的特异度,探索适合中国国情的HR-HPV筛查方案,包括筛查起始年龄、筛查间隔以及筛查异常的管理。
五、小结
1. HPV疫苗的应用将对HPV感染率和流行型别产生影响:
宫颈HSIL发生率下降;未覆盖型别感染率上升;覆盖型别感染率下降。
2. 后HPV疫苗时代,HPV检测更适合于筛查,细胞学检查则适于分流。
3. 未来可通过分型或载量及其他分流标记物来提升疫苗人群筛查的特异性。
4. 后疫苗时代筛查的合适起始年龄、安全间隔及如何整合疫苗与筛查策略,仍需要做更多研究。
5. 后疫苗时代,适合于我国国情的宫颈癌筛查策略仍有待探索。
【专家简介】

薛凤霞教授,医学博士,博士研究生导师,国务院特殊津贴专家,天津医科大学总医院妇产科主任。中华医学会妇产科分会常委,中国医师协会妇产科医师分会常委,天津市医师协会妇产科医师分会会长,中国优生科学协会副会长,中国优生科学协会生殖道疾病诊治分会主任委员,中华医学会妇科肿瘤学分会委员,中华医学会妇产科分会感染性疾病协作组副组长;《中华妇产科杂志》等多种核心期刊及全国高等医药院校规划教材《妇产科学》编委,《国际生殖健康/计划生育杂志》执行主编。
多年来致力于妇科肿瘤的临床与基础研究及女性生殖道感染的临床与基础研究,在妇科肿瘤的综合治疗、妇科疑难病例及女性生殖道感染性疾病的诊治方面经验丰富。从事妇产科教学工作近30年,承担本科生、硕士生、博士生及国际学院留学生的妇产科教学工作,参加全国高等医学院校教材《妇产科学》五年制5-9版、七年制及八年制等的编写。承担国家自然科学基金、教育部及天津市科委课题多项,发表中英文论著200余篇,其中SCI收录50余篇。相关科研成果获天津市科技进步一等奖1项,二等奖2项,三等奖2项;中华医学科技一等奖1项,华夏医学科技二等奖1项。
声明:本文为妇产科在线独家采编,经专家审阅后发布,如需转载,请注明出处!!!






 2020
2020 